Reação de Blaise
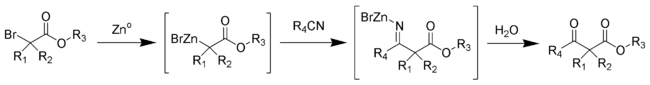
A reação de Blaise é uma reação orgânica que produz um β-cetoéster a partir da reação entre zinco metálico, um α-bromoéster e uma nitrila. A reação foi relatada pela primeira vez por Edmond Blaise (1872–1939) em 1901. O último intermediário é uma metaloimina, que é, então hidrolisada para fornecer o β-cetoéster desejado.
Ésteres alifáticos volumosos tendem a resultar em maiores rendimentos. Steven Hannick e Yoshito Kishi desenvolveram um procedimento aprimorado.
Notou-se uma tolerância a grupos hidroxila livres pno decorrer dessa reação, o que é surpreendente para reações de haletos organometálicos.
Mecanismo
O mecanismo da reação de Blaise envolve a formação de um complexo organozinco com o bromo na posição alfa da carbonila do éster. Isso torna o carbono alfa nucleofílico, permitindo que ele ataque o carbono eletrofílico do nitrilo. O nitrogênio nitrílico negativo resultante deste ataque forma um complexo com o cátion monobrometo de zinco. O produto β-enaminoéster (tautômero do intermediário imina ilustrado acima) é obtido por processamento com 50% de K2CO3 aquoso. Se o β-cetoéster for o produto desejado, a adição de ácido clorídrico 1 M hidrolisa o β-enaminoéster para converter a enamina em uma cetona, formando o β-cetoéster.

Ver também
Ligação externa
- Reação de Blaise - Detalhes e Literatura Recente (em inglês)
Referências
- ↑ Edmond E. Blaise; Compt. Rend. 1901, 132, 478.
- ↑ Rinehart, K. L., Jr. Organic Syntheses, Coll. Vol. 4, p. 120 (1963); Vol. 35, p. 15 (1955). (Article)
- ↑ Rao, H. S. P.; Rafi, S.; Padmavathy, K. Tetrahedron 2008, 64, 8037-8043. (Review)
- ↑ Cason, J.; Rinehart, K. L., Jr.; Thorston, S. D., Jr. J. Org. Chem. 1953, 18, 1594. (doi:10.1021/jo50017a022)
- ↑ Hannick, S. M.; Kishi, Y. J. Org. Chem. 1983, 48, 3833. (doi:10.1021/jo00169a053)
- [1] Marko, I.E. J. Am. Chem. Soc. 2007, ASAP doi:10.1021/ja0691728
- [2] Wang, D.; Yue, J.-M. Synlett 2005, 2077-2079.










