Diole
Diole – grupa organicznych związków chemicznych, alkohole zawierające dwie grupy hydroksylowe. Reaktywność dioli jest zbliżona do innych alkoholi.
Podział dioli
Diole wicynalne

Diole, w których grupy hydroksylowe przyłączone są do sąsiednich atomów węgla, noszą nazwę dioli wicynalnych lub (dawniej) glikoli[1][a]. Najprostszym ich przedstawicielem jest glikol etylenowy. Tetrapodstawione diole wicynalne są znane jako pinakole, a ich najprostszym reprezentantem jest pinakol (2,3-dimetylobutano-2,3-diol)[4][b].
Diole geminalne
Jeśli obie grupy hydroksylowe przyłączone są do jednego atomu węgla, związek nosi nazwę diolu geminalnego. Diole geminalne są zazwyczaj nietrwałe i ulegają spontanicznej dehydratacji do aldehydów lub ketonów; z tej przyczyny określane są często jako wodziany (hydraty) aldehydu/ketonu. Dehydratacja ta jest reakcją odwracalną:

- Równowaga acetaldehyd ⇌ 1,1-etanodiol
W niektórych przypadkach forma alkoholowa jest dominująca, np. w wodnym roztworze formaldehydu występuje głównie diol geminalny metanodiol, H
2C(OH)
2.
Nazewnictwo systematyczne
Nazwa dioli jest tworzona z nazwy odpowiedniego rodnika węglowodorowego przez dodanie do niego końcówki diol poprzedzonej, jeśli to konieczne, lokantami.
Przykłady:
-
 etano-1,2-diol (glikol etylenowy)
etano-1,2-diol (glikol etylenowy) -
 propano-1,3-diol
propano-1,3-diol -
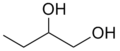 butano-1,2-diol
butano-1,2-diol -
 butano-1,3-diol
butano-1,3-diol -
 butano-1,4-diol
butano-1,4-diol -
 butano-2,3-diol
butano-2,3-diol -
 2-butyno-1,4-diol
2-butyno-1,4-diol -
 adamantano-1,3-diol
adamantano-1,3-diol
Zobacz też
 | Zobacz multimedia związane z tematem: Diole |
- alkohole wielowodorotlenowe
- przegrupowanie pinakolowe
Uwagi
- ↑ Nazwa glikole zazwyczaj dotyczy dioli wicynalnych, ale stosowane bywają także do innych dioli[2]. Zgodnie z zaleceniami nomenklaturowymi Międzynarodowej Unii Chemii Czystej i Stosowanej (IUPAC) z 2013 roku stosowanie takiej nazwy należy ograniczyć do niepodstawionego glikolu etylenowego[3].
- ↑ Zgodnie z zaleceniami nomenklaturowymi IUPAC z 2013 roku stosowanie takiej nazwy należy ograniczyć do niepodstawionego pinakolu[3].
Przypisy
- ↑ Robert T.R.T. Morrison Robert T.R.T., Boyd RobertB.R. N. Boyd RobertB.R., Chemia organiczna, t. 1, Warszawa: Państwowe Wydawnictwo Naukowe, 1985, s. 257–258, ISBN 83-01-04166-8 .
- ↑ glycols, [w:] A.D.A.D. McNaught A.D.A.D., A.A. Wilkinson A.A., Compendium of Chemical Terminology (Gold Book), S.J. Chalk (akt.), International Union of Pure and Applied Chemistry, wyd. 2, Oxford: Blackwell Scientific Publications, 1997, DOI: 10.1351/goldbook.G02654, ISBN 0-9678550-9-8 (ang.).
- ↑ a b P-63.1.1 Nazwy zachowane, [w:] Henri A.H.A. Favre Henri A.H.A., Warren H.W.H. Powell Warren H.W.H., Nomenklatura związków organicznych. Rekomendacje IUPAC i nazwy preferowane 2013, Komisja Terminologii Chemicznej Polskiego Towarzystwa Chemicznego (tłum.), wyd. 5, Narodowy Komitet Międzynarodowej Unii Chemii Czystej i Stosowanej, [2023], s. 646 .
- ↑ pinacols, [w:] A.D.A.D. McNaught A.D.A.D., A.A. Wilkinson A.A., Compendium of Chemical Terminology (Gold Book), S.J. Chalk (akt.), International Union of Pure and Applied Chemistry, wyd. 2, Oxford: Blackwell Scientific Publications, 1997, DOI: 10.1351/goldbook.P04674, ISBN 0-9678550-9-8 (ang.).
- GND: 4150017-9
- Catalana: 0099168, 0176395

















