Isobaar proces
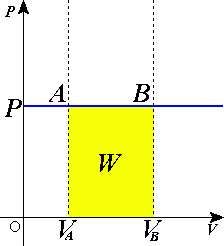
Een isobaar proces is een toestandsverandering van een bepaalde hoeveelheid materie waarbij de druk niet verandert, maar een of meer andere grootheden wel. Een voorbeeld hiervan is lucht in een cilinder met een vrij beweegbare zuiger waar warmte aan toegevoerd wordt. Door de temperatuurstijging zal het volume toenemen maar de druk niet.
Er gelden de volgende relaties:
Daarin is:
- de verrichte arbeid door de toestandsverandering (J)
- de toe- of afgevoerde hoeveelheid warmte (J)
- de druk (Nm-2)
- het volume (m³)
- de absolute temperatuur (K)
- de hoeveelheid stof (mol)
- de massa van de stof (kg)
- de soortelijke warmte van de stof bij constante druk ( J·kg-1·K-1)
- een verhoudingsgetal gelijk aan het quotiënt van de soortelijke warmte bij respectievelijk constante druk en constant volume
Zie ook
- Isotherm proces
- Isochoor proces





















