Méthylénation
Une méthylénation est une réaction chimique aboutissant à la liaison d'un groupe méthylène =CH2 à une molécule organique[1]. C'est par exemple le cas des réactions de Wittig[2] sur les aldéhydes et les cétones faisant intervenir des ylures de phosphore[3] :
- RCHO + Ph3P=CH2 ⟶ RCH=CH2 + Ph3PO.
Il est également possible de réaliser des méthylénations à l'aide du réactif de Tebbe (η5-C5H5)2Ti(µ-CH2)(µ-Cl)Al(CH3)2, suffisamment polyvalent pour traiter les esters[4] :
- RCOOR′ + Cp2Ti(CH2)(Cl)AlMe2 ⟶ RC(=CH2)OR′ + Cp2Ti(O)(Cl)AlMe2.
D'autres réactifs impliquant du titane, comme ceux de la méthylénation de Lombardo (en) (zinc, dibromométhane CH2Br2 et tétrachlorure de titane TiCl4 dans le tétrahydrofurane (THF)), permettent des réactions semblables[5],[6] :
Le réactif de Nysted C4H8O(BrZnCH2)2Zr fait également intervenir le TiCl4, avec le diéthyléthérate de trifluorure de bore BF3·OEt2, qui peut également être utilisé avec le dichlorure de titanocène (η5-C5H5)2TiCl2[7].
On a également utilisé des carbanions dérivés de méthylsulfones de manière semblable à la réaction de Wittig[8].
- Exemples de réactifs de méthylénation
-
 (C6H5)3P=CH2
(C6H5)3P=CH2 -

-
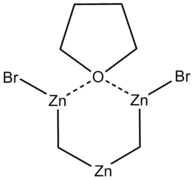
-
 (η5-C5H5)2TiCl2.
(η5-C5H5)2TiCl2.
Notes et références
- ↑ (en) Alejandro Bugarin, Kyle D. Jones et Brian T. Connell, « Efficient, direct α-methylenation of carbonyls mediated by diisopropylammonium trifluoroacetate », Chemical Communications, vol. 46, no 10, , p. 1715-1717 (DOI 10.1039/b924577d, lire en ligne).
- ↑ (en) Peter A. Byrne et Declan G. Gilheany, « The modern interpretation of the Wittig reaction mechanism », Chemical Society Reviews, vol. 42, no 16, , p. 6670-6696 (DOI 10.1039/c3cs60105f, lire en ligne).
- ↑ (en) Eric J. Leopold, « Selective hydroboration of a 1,3,7-triene: homogeraniol », Organic Syntheses, no 64, , p. 164 (DOI 10.15227/orgsyn.064.0164, lire en ligne).
- ↑ (en) Daniel A. Straus, M. Monzur Morshed, Matthew E. Dudley et M. Mahmun Hossain, « μ-Chlorobis(cyclopentadienyl)(dimethylaluminum)-μ-methylenetitanium », Encyclopedia of Reagents for Organic Synthesis, (DOI 10.1002/047084289X.rc073.pub2, lire en ligne).
- ↑ (en) Luciano Lombardo, « Methylenation of carbonyl compoundsM (+)-3-methylene-cis-p-menthane », Organic Syntheses, vol. 65, , p. 81 (DOI 10.15227/orgsyn.065.0081, lire en ligne).
- ↑ (en) Stephen P. Marsden et Pascal C. Ducept, « Synthesis of highly substituted allenylsilanes by alkylidenation of silylketenes », Beilstein Journal of Organic Chemistry, vol. 1, no 1, , p. 5 (PMID 16542018, PMCID 1399453, DOI 10.1186/1860-5397-1-5, lire en ligne
 ).
). - ↑ (en) Adam Haahr, Zoran Rankovic et Richard C. Hartley, « A one-pot procedure for methylenating carbonyl compounds using the Nysted reagent and titanocene dichloride », Tetrahedron Letters, vol. 52, no 23, , p. 3020-3022 (DOI 10.1016/j.tetlet.2011.04.017, lire en ligne).
- ↑ (en) Kaori Ando, Mai Oguchi, Takahisa Kobayashi, Haruka Asano et Nariaki Uchida, « Methylenation for Aldehydes and Ketones Using 1-Methylbenzimidazol-2-yl Methyl Sulfone », The Journal of Organic Chemistry, vol. 85, no 15, , p. 9936-9943 (PMID 32608238, DOI 10.1021/acs.joc.0c01227, lire en ligne).
 Portail de la chimie
Portail de la chimie
















