Cyanure de diéthylaluminium
| Cyanure de diéthylaluminium | |||
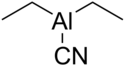 | |||
| Structure du cyanure de diéthylaluminium | |||
| Identification | |||
|---|---|---|---|
| No CAS | 5804-85-3 | ||
| No ECHA | 100.024.873 | ||
| No CE | 227-359-8 | ||
| PubChem | 16683962 | ||
| SMILES | CC[Al](CC)C#N PubChem, vue 3D | ||
| InChI | Std. InChI : vue 3D InChI=1S/2C2H5.CN.Al/c3*1-2;/h2*1H2,2H3;; Std. InChIKey : KWMUAEYVIFJZEB-UHFFFAOYSA-N | ||
| Propriétés chimiques | |||
| Formule | C5H10AlN | ||
| Masse molaire[1] | 111,121 1 ± 0,004 9 g/mol C 54,04 %, H 9,07 %, Al 24,28 %, N 12,6 %, | ||
| Propriétés physiques | |||
| Masse volumique | 0,864 g·cm-3[2] à 25 °C | ||
| Précautions | |||
| SGH[2] | |||
    Danger H225 : Liquide et vapeurs très inflammables H304 : Peut être mortel en cas d'ingestion et de pénétration dans les voies respiratoires H311 : Toxique par contact cutané H315 : Provoque une irritation cutanée H336 : Peut provoquer somnolence ou vertiges H361d : Susceptible de nuire au fœtus. H373 : Risque présumé d'effets graves pour les organes (indiquer tous les organes affectés, s'ils sont connus) à la suite d'expositions répétées ou d'une exposition prolongée (indiquer la voie d'exposition s'il est formellement prouvé qu'aucune autre voie d'exposition ne conduit au même danger) H410 : Très toxique pour les organismes aquatiques, entraîne des effets à long terme EUH032 : Au contact d'un acide, dégage un gaz très toxique P201 : Se procurer les instructions avant utilisation. P210 : Tenir à l’écart de la chaleur/des étincelles/des flammes nues/des surfaces chaudes. — Ne pas fumer. P273 : Éviter le rejet dans l’environnement. P280 : Porter des gants de protection/des vêtements de protection/un équipement de protection des yeux/du visage. P302 : En cas de contact avec la peau : P304+P340+P310 : En cas d'inhalation : transporter la victime à l’extérieur et la maintenir au repos dans une position où elle peut confortablement respirer. Appeler immédiatement un CENTRE ANTIPOISON/un médecin. | |||
| Transport[2] | |||
Numéro ONU : 3123 : LIQUIDE TOXIQUE, HYDRORÉACTIF, N.S.A. Classe : 4.3 Étiquettes :  4.3 : Matières qui, au contact de l'eau, dégagent des gaz inflammables  6.1 : Matières toxiques Emballage : Groupe d'emballage I : matières très dangereuses ; | |||
| Unités du SI et CNTP, sauf indication contraire. | |||
modifier  | |||
Le cyanure de diéthylaluminium, ou réactif de Nagata, est un composé organométallique de formule chimique ((CH3CH2)2AlCN)n. Il s'agit d'une substance incolore généralement manipulée en solution dans le toluène. Il est utilisé pour l'hydrocyanation des cétones α,β-insaturées[3],[4],[5],[6].
Préparation
Le cyanure de diéthylaluminium était initialement produit en traitant du triéthylaluminium (CH3CH2)6Al2 avec un léger excès de cyanure d'hydrogène HCN :
- n (CH3CH2)6Al2 + 2n HCN ⟶ 2 ((CH3CH2)2AlCN)n + 2n CH3CH3.
Le produit est généralement stocké dans des ampoules fermées car il est hautement toxique. Il se dissout dans le toluène, le benzène, l'hexane et l'éther diisopropylique. Il s'hydrolyse rapidement dans l'eau et n'est pas compatible avec les solvants protiques.
Structure
Le cyanure de diéthylaluminium n'a pas été cristallographié par rayons X bien que d'autres cyanures de diorganoaluminium l'ont été. Ces derniers présentent une formule générale (R2AlCN)n et existent sous forme de trimères ou de tétramères cycliques (n = 3 ou 4, respectivement). Ces oligomères ont des liaisons AlCN–Al.
Le cyanure de bis[di(triméthylsilyl)méthyl]aluminium (((CH3)3Si)2CH)2AlCN est semblable au cyanure de diethylaluminium. Son analyse cristallographique montre qu'il est trimérique avec la structure suivante[4] :

.
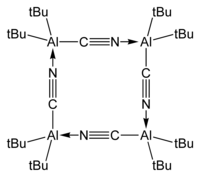
Le cyanure de bis(tert-butyl)aluminium ((CH3)3C)2AlCN existe sous forme tétramérique en phase cristallisée[7],[8] :
Applications
Le cyanure de diéthylaluminium est utilisé pour la réaction de Nagata, notamment l'hydrocyanation stœchiométrique des cétones α,β-insaturées. La réaction dépend de la basicité du solvant en raison du caractère acide du réactif[9]. Le but de cette réaction est de produire des alkylnitriles, qui sont précurseurs d'amines, d'amides, d'esters d'acides carboxyliques et d'aldéhydes.
-
 Exemple d'hydrocyanation.
Exemple d'hydrocyanation.
Notes et références
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- ↑ a b et c Fiche Sigma-Aldrich du composé Diethylaluminum cyanide solution 1.0 M in toluene, consultée le 7 mars 2021.
- ↑ (en) Wataru Nagata et Mitsuru Yoshioka, « Alkylaluminum cyanides as potent reagents for hydrocyanation », Tetrahedron Letters, vol. 7, no 18, , p. 1913-1918 (DOI 10.1016/S0040-4039(00)76271-X, lire en ligne)
- ↑ a et b (de) Werner Uhl, Uwe Schütz, Wolfgang Hiller et Maximilian Heckel, « Synthese und Kristallstruktur des trimeren [(Me3Si)2CH]2Al–CN », Zeitschrift für anorganische und allgemeine Chemie, vol. 621, no 5, , p. 823-828 (DOI 10.1002/zaac.19956210521, lire en ligne)
- ↑ (en) K. Wade et B. K. Wyatt, « Reactions of organoaluminium compounds with cyanides. Part III. Reactions of trimethylaluminium, triethylaluminium, dimethylaluminium hydride, and diethylaluminium hydride with dimethylcyanamide », Journal of the Chemical Society A: Inorganic, Physical, Theoretical, vol. 1969, , p. 1121-1124 (DOI 10.1039/J19690001121, lire en ligne)
- ↑ (en) G. E. Coates et R. N. Mukherjee, « 35. Dimethylaluminium cyanide and its gallium, indium, and thallium analogues; beryllium and methylberyllium cyanide », Journal of the Chemical Society (Resumed), vol. 1963, , p. 229-233 (DOI 10.1039/JR9630000229, lire en ligne)
- ↑ (en) Werner Uhl et Madhat Matar, « Hydroalumination of Nitriles and Isonitriles », Zeitschrift für Naturforschung, vol. 59, , p. 1214-1222 (lire en ligne)
- ↑ (en) Klaus Knabel et Heinrich Nöth, « Synthesis and Structures of Some Aluminum Pseudohalides », Zeitschrift für Naturforschung, vol. 60, , p. 155-163 (lire en ligne)
- ↑ (en) W. Nagata et M. Yoshioka, « Diethylaluminum cyanide », Organic Syntheses, vol. 52, , p. 90 (DOI 10.15227/orgsyn.052.0090, lire en ligne)
 Portail de la chimie
Portail de la chimie










