Adiponitrile

Pour les articles homonymes, voir ADN (homonymie).
| Adiponitrile | |||
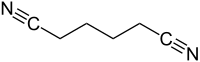 Structure de l'adiponitrile. | |||
| Identification | |||
|---|---|---|---|
| Nom UICPA | hexanedinitrile | ||
| No CAS | 111-69-3 | ||
| No ECHA | 100.003.543 | ||
| No CE | 203-896-3 | ||
| No RTECS | AV2625000 | ||
| PubChem | 8128 | ||
| SMILES | C(CCC#N)CC#N PubChem, vue 3D | ||
| InChI | InChI : vue 3D InChI=1S/C6H8N2/c7-5-3-1-2-4-6-8/h1-4H2 InChIKey : BTGRAWJCKBQKAO-UHFFFAOYSA-N | ||
| Propriétés chimiques | |||
| Formule | C6H8N2 [Isomères] | ||
| Masse molaire[1] | 108,141 1 ± 0,005 8 g/mol C 66,64 %, H 7,46 %, N 25,9 %, | ||
| Propriétés physiques | |||
| T° fusion | 2,3 °C[2] | ||
| T° ébullition | 295 °C[2] | ||
| Solubilité | 50 g l−1[2] à 20 °C | ||
| Masse volumique | 0,96 g cm−3[2] | ||
| T° d'auto-inflammation | 460 °C[2] | ||
| Point d’éclair | 165 °C[2] | ||
| Pression de vapeur saturante | 0,3 Pa[2] à 20 °C | ||
| Thermochimie | |||
| ΔfH0gaz | 149,0 kJ mol−1[réf. souhaitée] | ||
| ΔfH0liquide | 85,0 kJ mol−1[3] | ||
| ΔfusH° | 18,0 kJ mol−1[4] | ||
| Propriétés optiques | |||
| Indice de réfraction | 1,438[réf. souhaitée] | ||
| Précautions | |||
| SGH[2] | |||
 Danger H301 : Toxique en cas d'ingestion H315 : Provoque une irritation cutanée H319 : Provoque une sévère irritation des yeux H332 : Nocif par inhalation P302+P352 : En cas de contact avec la peau : laver abondamment à l’eau et au savon. P305+P351+P338 : En cas de contact avec les yeux : rincer avec précaution à l’eau pendant plusieurs minutes. Enlever les lentilles de contact si la victime en porte et si elles peuvent être facilement enlevées. Continuer à rincer. P309+P311 : En cas d'exposition ou de malaise : appeler immédiatement un CENTRE ANTIPOISON ou un médecin. | |||
| Transport[2] | |||
Code Kemler : 60 : matière toxique ou présentant un degré mineur de toxicité Numéro ONU : 2205 : ADIPONITRILE Classe : 6.1 Étiquette :  6.1 : Matières toxiques Emballage : Groupe d'emballage III : matières faiblement dangereuses. | |||
| Écotoxicologie | |||
| DL50 | 300 mg kg−1 (souris, oral)[réf. souhaitée] | ||
| Unités du SI et CNTP, sauf indication contraire. | |||
modifier  | |||
L'adiponitrile (ADN) est un composé organique hautement toxique (il fait partie de la liste EPA des substances extrêmement dangereuses), de formule N≡C(–CH2)4–C≡N. Il s'agit d'un dinitrile se présentant sous la forme d'un liquide incolore et visqueux, intermédiaire de la synthèse des polyamides.
Synthèse
Du fait de son importance pour l'industrie chimique, de nombreuses voies de synthèse ont été développées.
Deux procédés sont principalement utilisés aujourd'hui[5] :
- le procédé Invista (société Dupont) qui part de butadiène et d'acide cyanhydrique ;
- le procédé Ascend (société Monsanto) qui utilise l'acrylonitrile comme molécule de départ.
Procédé Invista
L'adiponitrile est produit de nos jours essentiellement par hydrocyanation du 1,3-butadiène H2C=CH–CH=CH2 catalysée par le nickel, selon un procédé découvert chez DuPont, la réaction globale est :
- H2C=CH–CH=CH2 + 2 HCN → N≡C(–CH2)4–C≡N
Cette réaction se fait en plusieurs étapes, tout d'abord une hydrocyanation qui produit des pentène-nitriles et des méthylbutanenitriles :

Une isomérisation permet de convertir les méthylbutanenitriles en pentènenitriles. Puis une seconde hydrocyanation conduit à la formation de l'adiponitrile :

Ce procédé est mis en œuvre par la société Butachimie dans l'usine de Chalampé en Alsace. Cette usine produit 35 % de l'adiponitrile mondial[6].
Procédé Ascend
L'autre procédé est l'électrosynthèse par dimérisation de l'acrylonitrile CH2=CH–C≡N, découverte chez Monsanto :
- 2 CH2=CH–C≡N + 2 e− + 2 H+ → N≡C(–CH2)4–C≡N.
Utilisations
Production de l'hexaméthylènediamine H2N(–CH2)6NH2 par hydrogénation :
- N≡C(–CH2)4–C≡N + 4 H2 → H2N(–CH2)6NH2.
Notes et références
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- ↑ a b c d e f g h i et j Entrée « Adiponitrile » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 22 novembre 2012 (JavaScript nécessaire).
- ↑ Lebedeva, N.D., Katin et Yu.A., « Heats of combustion of oenanthonitrile, adiponitrile, and tetramethylsuccinodinitrile », Russ. J. Phys. Chem. (Engl. Transl.), vol. 47, , p. 922.
- ↑ E. Badea, I. Blanco et G. Della Gatta, « Fusion and solid-to-solid transitions of a homologous series of alkane-α,ω-dinitriles », Journal of Chemical Thermodynamics, vol. 39(10), , p. 1392-1398 (lire en ligne).
- ↑ (en) Alexander, Tullo, « The chemical industry is bracing for a nylon 6,6 shortage », Chemical & Engineering News, vol. 96 (40), (lire en ligne).
- ↑ « Butachimie ».
 Portail de la chimie
Portail de la chimie













